Seit mehreren Jahren können Forschende an der Julius-Maximilians-Universität (JMU) und dem Helmholtz-Institut Würzburg (HIRI) einzelnen Zellen bei der Arbeit zusehen: Der Wissenschaftsstandort Würzburg verfügt mit dem Single-Cell Center (SCC) über hochmoderne Expertise in der experimentellen und computergestützten Einzelzellanalyse. Mit dem neuen „In-situ-RNA-Imaging-Analyzer“ lassen sich jetzt auch die komplexen Abläufe von Krankheiten sichtbar machen.
Lange war die Einzelzellanalyse wie ein Blick durch ein Schlüsselloch: Man konnte sehen, welche Eigenschaften eine einzelne Zelle besitzt. Die Umgebung sah man allerdings nicht, räumliche Informationen fehlten bislang: Welche Rolle spielt die Nachbarzelle? Wie beeinflussen sich Zellen gegenseitig, wenn sie dicht an dicht in einem Gewebe liegen?
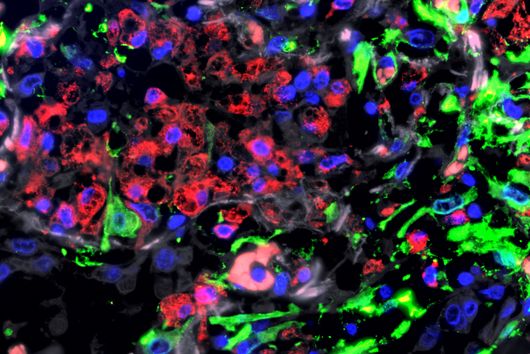
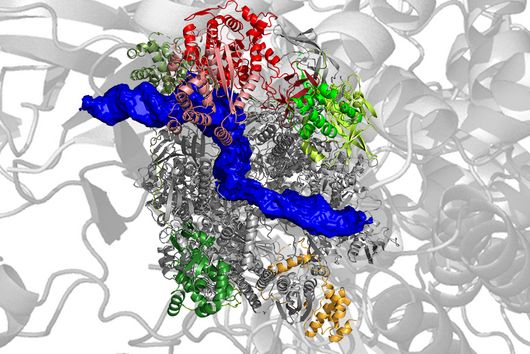
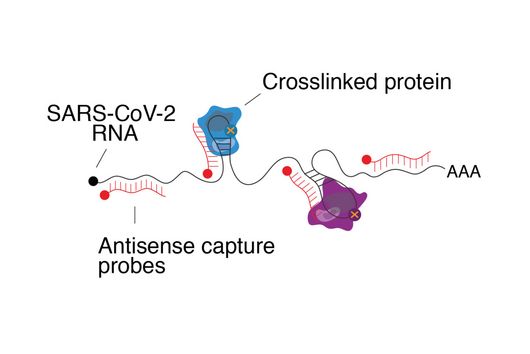
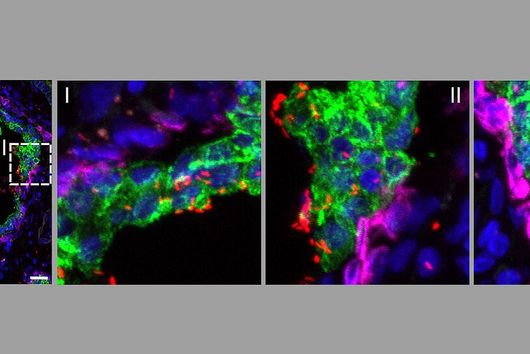
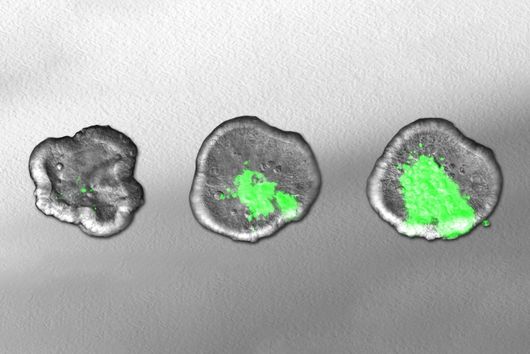
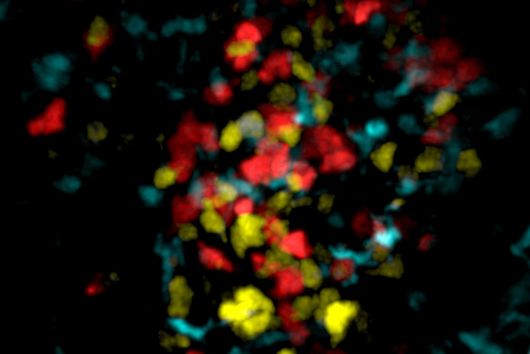
Diese Lücke kann nun geschlossen werden: Ein neues High-End-Gerät ermöglicht es Würzburger Forschenden jetzt, Gewebe besser zu analysieren. „Der In-situ-RNA-Imaging-Analyzer ist für uns ein leistungsstarkes Werkzeug. Er erlaubt es, die räumliche Verteilung von RNA-Molekülen in Zellen und Geweben sichtbar zu machen und damit biologische Prozesse wesentlich genauer zu verstehen“, erklärt Dominic Grün, Inhaber des Lehrstuhls für Computational Biology of Spatial Biomedical Systems und stellvertretender Sprecher des Single-Cell Centers.

[Translate to German:] From left to right: Fabian Imdahl (Project Manager and Application Specialist at the SCC), Dominic Grün, Tobias Krammer (Spatial Transcriptomics Specialist and Coordinator for the SFB DECIDE / Cardio Single-Cell Projects at the SCC) and Emmanuel Saliba in front of the new state-of-the-art “In-situ RNA Imaging Analyzer.” © HIRI / Luisa Härtig
Antoine-Emmanuel Saliba, Sprecher des Single-Cell Centers und Forschungsgruppenleiter am Helmholtz-Institut für RNA-basierte Infektionsforschung, unterstreicht die strategische Bedeutung: „Mit dieser Investition positioniert sich Würzburg als Vorreiter in der Einzelzellforschung. Das Single-Cell Center stellt nicht nur modernste Methoden bereit, sondern auch das Know-how, um Daten effizient auszuwerten, und schafft damit ideale Voraussetzungen, um die Forschung am Standort nachhaltig zu stärken.“
Neue Einblicke in Krankheitsabläufe
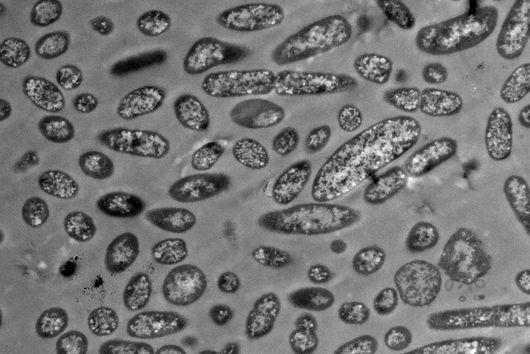
So lässt sich beispielsweise das Knochenmark von Patient:innen mit Multiplem Myelom, einer Form von Knochenmarkkrebs, genauer untersuchen. Forschende können identifizieren, welche Zellen an der Erkrankung beteiligt sind und durch welche molekularen Mechanismen sie sich gegenseitig beeinflussen. Molekulare Wechselwirkungen zwischen Zellen haben einen wesentlichen Einfluss auf den Krankheitsverlauf und auf die Regeneration des Gewebes nach erfolgter Therapie, und diese Mechanismen können nun mit dieser neuen Technologie entschlüsselt werden.
Ein weiteres Anwendungsbeispiel ist die Heilung nach einem Herzinfarkt. Hier bildet sich Narbengewebe, wodurch das Herz an Pumpkraft verliert. Das kann langfristig zu Herzschwäche oder Herzversagen führen. Wüsste man, wie beteiligte Zellen im Verbund die Reparatur des Herzgewebes steuern, könnten künftige Therapien die Heilung gezielt unterstützen.
Die neue Technologie verschiebt die Grenzen dessen, was über Krankheiten wie Krebs, Autoimmunstörungen oder Infektionen bekannt ist. Sie erfordert aber zugleich hohe technische Expertise: Die enormen Datenmengen werden mithilfe von Machine Learning und Künstlicher Intelligenz ausgewertet. Die Teams um Dominic Grün und Emmanuel Saliba nutzen und entwickeln spezielle Algorithmen, um die Informationen sinnvoll zu interpretieren.





















![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/b/9/csm_Jahresrueckblick_2025_963859644e.jpg)








![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/e/6/csm_2025_11_20_Neubaufuehrung_fuer_Mitarbeitende_c_HIRI_Yara_Huisl_06_low_0cac9755ff.jpg)
















































![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/5/4/csm_2024_10_EUREKA__c_HIRI_Luisa_Macharowsky_3_low_01_863006bd0e.jpg)































![[Translate to German:]](/fileadmin/HIRI/__processed__/3/3/csm_2022_07_BEISEL_Chase_2_cropped_Low_a7a341cf03.jpg)





































![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/2/8/csm_Collage_WUE_9fa1cd516c.jpg)










![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/0/8/csm_05_Saliba_02_c_HIRI_Luisa_Macharowsky_ohne_Lacoste_low_zugeschnitten_2_01_9822d73a3f.jpg)






![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/c/c/csm_HIRI-Grundstseinlegung_Foto__c_Mario_Schmitt_79ad64af6d.jpg)













![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/c/2/csm_2023_04_Smyth_Paper_c_HIRI_Luisa_Macharowsky_2_low_84f993d581.jpg)





























![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/e/2/csm_2022_11_HIRI_City_of_Wuerzburg_Child_Care_c_HIRI_Luisa_Macharowsky_2_low_6445b253eb.jpg)
![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/3/9/csm_HIRI_key_visual_CHurtig_606d992d74.jpg)





























![[Translate to German:] [Translate to German:]](/fileadmin/HIRI/__processed__/f/0/csm_Ahsen_blue2_6e28a4ee6b.jpg)












![[Translate to Deutsch:] [Translate to Deutsch:]](/fileadmin/HIRI/__processed__/a/5/csm_2022_02_Marco_Olguin_HIRI-Luisa_Macharowsky_04_low_new_3dc837191c.jpg)


![[Translate to Deutsch:] [Translate to Deutsch:]](/fileadmin/HIRI/__processed__/3/c/csm_Joerg_Vogel_Portrait_-_photocredit_Mario_Schmitt__c__HIRI_5013b9643b.jpg)



![[Translate to Deutsch:] [Translate to Deutsch:]](/fileadmin/HIRI/__processed__/a/6/csm_RNA_Delivery_1902376336.jpg)
![[Translate to Deutsch:]](/fileadmin/HIRI/__processed__/7/c/csm_Caliskan_Kibe_Pekarek_105c7d1860.jpg)
![[Translate to Deutsch:] [Translate to Deutsch:]](/fileadmin/HIRI/__processed__/c/1/csm_N-Caliskan_M-Zimmer_Zoom_c93c493293.jpg)